Khẩu trang y tế là một loại mặt nạ bao bọc vùng mũi, miệng của người sử dụng. Nhằm mục đích bảo vệ họ khỏi các loại hạt trong không khí, vi khuẩn, dịch bệnh lây qua đường hô hấp. Khẩu trang y tế nói chung và khẩu trang y tế kháng khuẩn nói riêng là loại thiết bị bảo hộ thiết yếu tại các cơ sở khám chữa bệnh. Hoa Kỳ là một trong những thị trường tiềm năng cho các nhà xuất khẩu khẩu trang y tế. Bài viết dưới đây sẽ trình bày những quy định của FDA – Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ về đăng ký FDA cho khẩu trang y tế và khẩu trang y tế kháng khuẩn.
Phân loại khẩu trang
Theo quy định của FDA, khẩu trang y tế được chia thành nhiều mã sản phẩm. Song nhìn chung có hai nhóm lớn như sau:
Khẩu trang y tế không kháng khuẩn
Đối với khẩu y tế không kháng khuẩn bao gồm 2 loại : Khẩu trang lọc và Khẩu trang ngoại khoa/phẫu thuật.
Khẩu trang ngoại khoa/Khẩu trang phẫu thuật (Surgical mask)
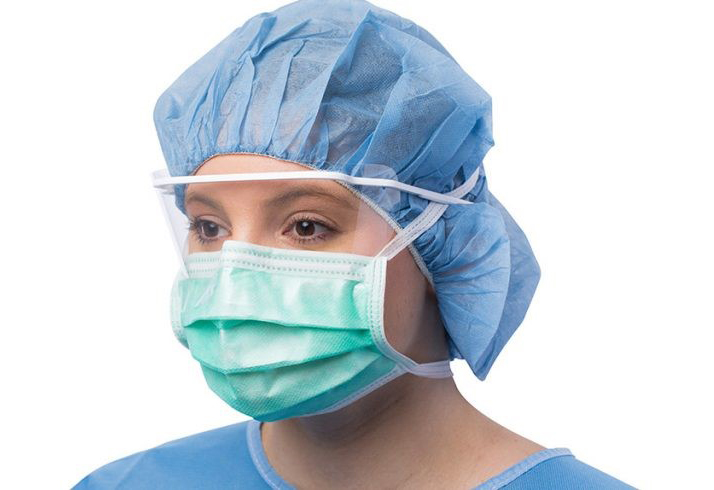
Khẩu trang ngoại khoa là thiết bị dùng một lần, không ôm sát. Nó tạo ra một rào cản vật lý giữa miệng và mũi của người đeo và các chất gây ô nhiễm tiềm ẩn trong môi trường xung quanh. Loại khẩu trang này không được dùng chung và có thể được dán nhãn là khẩu trang phẫu thuật, cách ly, nha khoa hoặc thủ thuật y tế. Khẩu trang ngoại khoa thường được gọi là khẩu trang y tế. (Nhưng không phải loại khẩu trang y tế nào cũng là khẩu trang ngoại khoa).
Khi được đeo đúng cách, khẩu trang ngoại khoa sẽ giúp chặn các hạt nước lớn, dịch phun, văng hoặc bắn mà có thể chứa vi trùng, vi rút và vi khuẩn, ngăn không cho chúng xâm nhập vào mũi, miệng người đeo. Đồng thời, nó có thể giúp ngăn nước bọt, dịch tiết của người đeo lây nhiễm ra môi trường qua hành động ho, hắt hơi,…Tuy nhiên, khẩu trang ngoại khoa không thể chặn những hạt siêu nhỏ trong không khí. Và do không ôm sát nên loại khẩu trang này cũng không thể ngăn hoàn toàn các loại vi khuẩn và các chất gây ô nhiễm khác.
Phần lớn khẩu trang phẫu thuật là loại không kháng khuẩn. Vì công dụng chủ yếu của khẩu trang phẫu thuật là ngăn chất lỏng, giọt bắn. Vì những tính năng này mà khẩu trang ngoại khoa là sản phẩm có số lượng tiêu thụ cao nhất kể từ khi đại dịch Covid bùng phát đến nay.
Khẩu trang lọc (Respirator), phổ biến nhất là Khẩu trang N95
Khẩu trang N95 là một thiết bị bảo vệ đường hô hấp được thiết kế để giúp lọc rất hiệu quả các hạt trong không khí, giọt bắn và dịch tiết hệ hô hấp. Lưu ý rằng các cạnh của khẩu trang được thiết kế để tạo thành một dấu niêm phong xung quanh mũi và miệng. Đây là điểm khác biệt nhất giữa khẩu trang N95 và khẩu trang y tế thông thường. Loại khẩu trang này có khả năng lọc ít nhất 95% hạt to, nhỏ trong không khí, bảo vệ người đeo hiệu quả trước các loại vi rút, vi khuẩn khi được đeo vừa vặn với mặt người sử dụng.

Khẩu trang N95 dùng trong y tế được sử dụng bởi nhân viên chăm sóc sức khỏe trong quá trình làm thủ thuật để bảo vệ bệnh nhân và cả chính họ khỏi sự lây truyền của vi sinh vật, dịch cơ thể và vật chất dạng hạt.
Khẩu trang y tế kháng khuẩn
Đây là loại khẩu trang y tế có thành phần kháng khuẩn, bao gồm cả loại khẩu trang ngoại khoa và khẩu trang lọc N95. Thành phần kháng khuẩn của khẩu trang là vải được xử lý bằng những chất phụ gia có tác dụng kháng khuẩn trong quá trình sản xuất. Vải sau khi được xử lý kháng khuẩn thì sẽ ngăn ngừa sự phát triển và lây lan của vi sinh vật trong vải. Kể cả vi khuẩn, vi rút lây nhiễm lên bề mặt khẩu trang trong quá trình sử dụng cũng có thể bị tiêu diệt.
Các thành phần kháng khuẩn được dùng trong khẩu trang phải được FDA xem xét trước khi được đưa vào thị trường. Nhà sản xuất sẽ cần giải trình về loại vi khuẩn được nhắm tới và khả năng chất kháng khuẩn làm sinh ra chủng vi khuẩn kháng thuốc.
Quy định của FDA đối với khẩu trang y tế và khẩu trang lọc
FDA có quy định cụ thể đối với từng loại khẩu trang.
Khẩu trang không dùng cho mục đích y tế
Trước tiên, FDA sẽ chỉ yêu cầu đăng ký đối với khẩu trang là thiết bị y tế. Tức là khẩu trang, dù là chủng loại gì, phải nhằm mục đích sử dụng trong việc chẩn đoán bệnh tật hoặc các tình trạng khác, hoặc trong việc chữa bệnh, giảm nhẹ, điều trị hoặc ngăn ngừa bệnh tật ở người hoặc động vật khác.
FDA chỉ quan tâm quản lý đến khẩu trang y tế dùng cho mục đích y tế vì chúng có ảnh hưởng trực tiếp đến sức khỏe cộng đồng. Nếu sản phẩm không được đảm bảo chất lượng thì sẽ có nguy cơ gây nguy hiểm đến sức khỏe, tính mạng của người sử dụng và thậm chí là đến cộng đồng xung quanh.
Những loại khẩu trang không được sử dụng cho mục đích y tế (như dùng trong xây dựng hoặc các nhà máy công nghiệp) thì sẽ không được coi là thiết bị y tế. Do đó chúng không thuộc phạm vi quản lý của FDA và không cần phải được đăng ký để nhập khẩu vào thị trường Hoa Kỳ. FDA đánh giá loại sản phẩm này gần như không có ảnh hưởng đến sức khỏe người tiêu dùng.
Tất cả các cơ sở muốn xuất khẩu sản phẩm khẩu trang y tế vào thị trường Hoa Kỳ đều phải làm thủ tục đăng ký FDA. Đây là thủ tục giúp FDA thực hiện quản lý về chất lượng sản phẩm và truy xét trách nhiệm nếu có sai phạm xảy ra sau khi sản phẩm vào thị trường. Tùy vào phân loại của từng sản phẩm, nhà xuất khẩu sẽ xác định được những quy định mà sản phẩm cần tuân thủ và những nội dung cần có để có thể thực hiện đăng ký FDA.
Đối với khẩu trang y tế (mã sản phẩm: FXX) và khẩu trang y tế kháng khuẩn (mã sản phẩm: OUK)
Sản phẩm khẩu trang y tế thường và khẩu trang y tế kháng khuẩn đều được phân vào nhóm thiết bị y tế loại II theo quy định của FDA.
Hồ sơ đăng ký FDA của thiết bị y tế loại II có yêu cầu thư xác nhận Thông báo trước thị trường – 510k từ FDA. Để nhận được thư xác nhận này, nhà xuất khẩu cần phải nộp cho FDA một bản Thông báo trước thị trường – 510k. Về cơ bản, 510k là một bản đệ trình trước khi tiếp cận thị trường được gửi cho FDA. Nhằm để chứng minh rằng thiết bị được tiếp thị là an toàn và hiệu quả, “tương đương đáng kể” với thiết bị đã được tiếp thị hợp pháp theo quy định Mỹ. Không có một mẫu tiêu chuẩn nào cho 510k. Người nộp phải so sánh thiết bị của họ với một hoặc nhiều thiết bị tương tự được tiếp thị hợp pháp và đưa ra lập luận và bằng chứng cho sự tương đương này.
Quy trình đăng ký 510k sẽ diễn ra trong vòng 90 ngày kể từ ngày FDA nhận đủ thông tin và tài liệu được yêu cầu. Vậy nên FDA khuyến nghị doanh nghiệp nên nộp 510k trước khi tạo tài khoản đăng ký FDA ít nhất 3 tháng.
Ngoài ra khẩu trang y tế mã FXX và OUK còn phải tuân thủ quy định chung về ghi nhãn sản phẩm. Trên nhãn sản phẩm cần phải có những thông tin như: tên sản phẩm; tên và trụ sở của nhà sản xuất, nhà đóng gói hoặc nhà phân phối; mục đích sử dụng; hướng dẫn sử dụng đầy đủ;…
Đối với Khẩu trang lọc N95 (mã sản phẩm: MSH) và N95 kháng khuẩn (mã sản phẩm: ONT)
Khẩu trang lọc N95 và khẩu trang N95 kháng khuẩn đều là thiết bị y tế loại II theo quy định của FDA. Hồ sơ đăng ký FDA cũng các sản phẩm cũng có yêu cầu về 510k như đã nêu ở phần trước. Khẩu trang lọc N95 cũng phải tuân thủ yêu cầu về ghi nhãn sản phẩm.
Tuy nhiên FDA có quy định miễn trừ 510k cho khẩu trang N95 mã MSH nếu không thuộc trường hợp sau:
- Khẩu trang nhằm ngăn ngừa một số bệnh cụ thể hoăc nhiễm trùng
- Khẩu trang được ghi nhãn hoặc tiếp thị là có thể lọc khói trong phẫu thuật, lọc một lượng vi rút hoặc vi khuẩn cụ thể, làm giảm số lượng và/hoặc tiêu diệt vi rút, vi khuẩn hoặc nấm hoặc ảnh hưởng đến khả năng gây dị ứng, hoặc
- Khẩu trang chứa các công nghệ phủ không liên quan đến lọc (ví dụ: để giảm và hoặc tiêu diệt vi sinh vật).
Chính sách của FDA cho trường hợp khẩn cấp
Trong trường hợp thị trường đột nhiên thiếu hụt nguồn cung thiết bị y tế hoặc có tình trạng khẩn cấp về sức khỏe cộng đồng (như tình trạng đại dịch Covid hiện nay), FDA ban hành một chính sách tạm thời dành cho các loại khẩu trang và mặt nạ.
Theo chính sách này, khi thiếu hụt nguồn cung khẩu trang, FDA sẽ cho phép phân phối và sử dụng các loại khẩu trang, mặt nạ mà thuộc các trường hợp sau:
- Khẩu trang dùng cho mục đích y tế nhưng không chống thấm: sản phẩm phải thỏa mãn tiêu chí của EUA, chưa cần nộp 510k.
- Khẩu trang y tế / khẩu trang ngoại khoa có chống thấm: chưa cần nộp 510k nhưng phải ghi nhãn cảnh báo đầy đủ.
- Khi khẩu trang N95 do FDA thông qua hoặc được NIOSH phê chuẩn không có sẵn trên thị trường: cho phép thay thế bằng N95 đạt tiêu chuẩn của quốc gia mà được đánh giá bằng phương pháp giống với của NIOSH, thỏa mãn tiêu chí của EUA, chưa cần nộp 510k.
Những trường hợp nói trên sẽ được phân thành mã sản phẩm mới dùng trong thời kỳ khẩn cấp, khi qua thời gian này sẽ bị loại bỏ. Riêng đối với khẩu trang y tế có thành phần kháng khuẩn, dù sản phẩm có được ghi nhãn kháng khuẩn hay không, thì đều phải nộp 510k để được bán trên thị trường Hoa Kỳ. Sở dĩ yêu cầu như vậy vì FDA muốn phòng ngừa sự xuất hiện của những chủng vi khuẩn kháng thuốc.
Đăng ký FDA cho khẩu trang y tế và khẩu trang kháng khuẩn tại G-GLOBAL
Với mong muốn giúp đỡ các nhà xuất khẩu đưa sản phẩm vào thị trường Hoa Kỳ, G-GLOBAL trân trọng cung cấp dịch vụ hỗ trợ nhà xuất khẩu làm thủ tục đăng ký FDA cho các loại hàng hóa, trong đó có khẩu trang y tế và khẩu trang kháng khuẩn.
Vì sao nên chọn G-GLOBAL?
- G-GLOBAL cung cấp dịch vụ với giá cả cạnh tranh.
- G-GLOBAL có đội ngũ giàu kinh nghiệm trong lĩnh vực đăng ký FDA cho thiết bị y tế nói chung và khẩu trang y tế nói riêng. Nhân viên sẵn sàng tư vấn và giải đáp thắc mắc miễn phí.
- G-GLOBAL có đối tác uy tín chuyên cung cấp dịch vụ Đại lý tại Hoa Kỳ, giúp khách hàng nhanh chóng chỉ định Đại lý Hoa Kỳ (một yêu cầu bắt buộc trong thủ tục đăng ký FDA) với giá cả tối ưu.
Nếu có bất kỳ thắc mắc nào về đăng ký FDA cho khẩu trang y tế và khẩu trang y tế kháng khuẩn vui lòng liên hệ theo phương thức sau:
Địa chỉ: Tầng 7 Tòa nhà HLT Số 23 Ngõ 37/2 Dịch Vọng Cầu Giấy Hà Nội
Điện thoại: 0985.422.225
Email: gglobal@gmail.com